Hastaların Aduhelm (aducanumab) hakkında bilmesi gereken her şey | New Alzheimer's Medicine
Son Güncelleme 15 Mart 2022

Ülkenizde onaylanmamış olsalar bile yeni ilaçlara yasal olarak erişebilirsiniz.
Nasıl olduğunu öğreninMakale Dr. Jan de Witt tarafından gözden geçirildi
7 Haziran 2021'de FDA 'nın Alzheimer hastalığının tedavisi için aducanumab 'ı ("Aduhelm" ticari adıyla üretilmektedir) onaylaması, dünya çapında milyonlarca Alzheimer hastası ve ailesinin umutlarını artırırken, uzmanlar karara ilişkin endişelerini dile getirdi.
Aduhelm , Alzheimer hastalığı için 18 yıl içinde FDA tarafından onaylanan ilk ilaçtır Bu ilaç, yayınlanan sonuçlara göre, Alzheimer hastalığının semptomlarını hafifletmekten ziyade ilerlemesini yavaşlatabildiğini iddia etmektedir.
FDA'nın ilacı onaylama kararı tartışmalarla dolu. Bununla birlikte, Aduhelm'in üreticisi Biogen, Haziran 2021'in sonuna kadar Aduhelm 'i Amerika Birleşik Devletleri'ndeki 900'den fazla sağlık merkezine göndermeye başlamayı bekliyor.
Aduhelm şu anda Amerika Birleşik Devletleri dışındaki uygun hastalar için merhametli kullanım veya belirlenmiş hasta bazında mevcuttur. " Aduhelm 'eAmerika Birleşik Devletleri Dışında Erişim" bölümüne geçerek daha fazla bilgi edinin.
Alzheimer hastalığı: 21. yüzyılın en büyük sosyal, tıbbi ve ekonomik krizlerinden biri
Alzheimer hastalığı, günümüzde dünya çapında 40 milyondan fazla insanı etkileyen ve bunamanın en yaygın nedeni olan dejeneratif bir beyin hastalığıdır. Uzun yıllar boyunca yaşlanmanın normal bir parçası olduğuna inanılan Alzheimer hastalığı, artık ciddi sağlık, ekonomik ve sosyal etkileri olan bir durum olarak kabul edilmektedir.
Araştırmacılar Alzheimer hastalığına neyin neden olduğunu henüz tam olarak anlamış değiller, ancak hastalığa aşağıdaki gibi faktörlerin bir araya gelmesinin neden olduğuna inanılıyor:
- Yaşlanma: Alzheimer en sık 65 yaşından sonra teşhis edilir (geç başlangıçlı Alzheimer hastalığı). Yaşı 85 ve üzerinde olan kişilerin yaklaşık üçte birinde Alzheimer hastalığı vardır. Yaşlanmaya bağlı olarak beyinde meydana gelen değişiklikler bu durumun gelişmesine katkıda bulunabilir.
- Aile geçmişi: Birinci dereceden Alzheimer hastası bir aile üyesine sahip olmak, bir kişinin hastalığa yakalanma riskini artırır. Bilim insanları, genetik yatkınlığın 30'lu yaşlardan 60'lı yaşların ortalarına kadar olan kişilerde görülen erken başlangıçlı Alzheimer'a neden olabileceğine inanmaktadır. Alzheimer hastalarının sadece %10'u hastalığın erken başlangıçlı formuna sahiptir.
- Diğer faktörler: Bilim insanları bilişsel gerileme ile kalp hastalığı, diyabet ve obezite arasında bağlantılar bulmuşlardır. En güçlü kanıtlar beyin sağlığı ile kalp sağlığı arasında bağlantı kurmaktadır. Kafa travmaları da amiloid plaklarının oluşumunu tetikleyebildiği için Alzheimer riskinin artmasıyla ilişkilendirilmiştir. Fazladan bir kromozomun Alzheimer ile bağlantılı bir tür amiloid proteini için genetik kodlamayı belirlediği Down sendromlu kişiler de yüksek risk altındadır.
Alzheimer hastalarının çoğunluğu, bazı belirtilerin tanıdan on yıl önce bile ortaya çıkmaya başlamasına rağmen, belirtilerin daha belirgin hale geldiği ve hastalığın beyinde bir miktar hasara neden olduğu hafif evrede teşhis edilir. Erken belirtiler hastalar tarafından göz ardı edilebilir (genellikle utanç nedeniyle) veya doktorlar ya da aile üyeleri tarafından fark edilmeyebilir. Hastaların tanıdan sonra ortalama yaşam beklentisi 3-11 yıldır.
"Zamanla annem kim olduğumu unuttu."
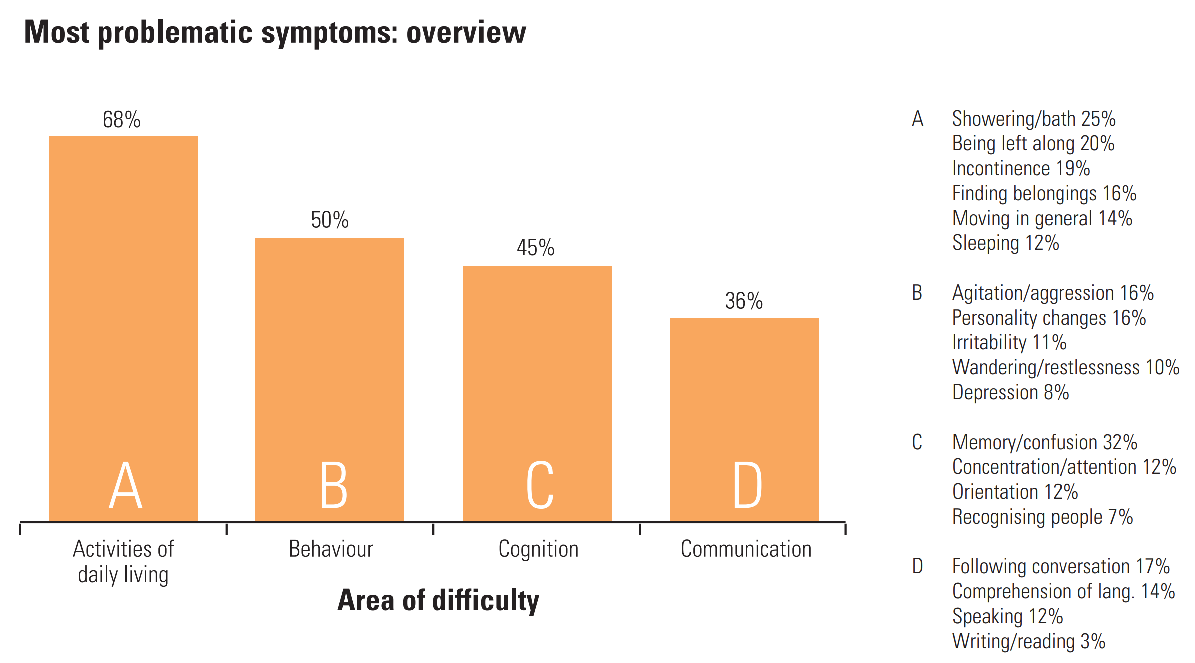
Alzheimer hastalığının üç farklı evresi vardır:
- Hafif: İlk aşamalarda, hastalar önemli tarihleri ve olayları unutma, soruları sık sık tekrarlama, günlük işleri tamamlamanın daha uzun sürmesi, mali konularda sürekli sorun yaşama, eşyaları sık sık yanlış yere koyma ve endişe gibi hafıza kaybı yaşarlar. (Yaşlanmayla birlikte ne kadar hafıza kaybının normal olduğu hakkında daha fazla bilgi edinmek için Ulusal Sağlık Enstitüleri'nin (NIH) Ulusal Yaşlanma Enstitüsü tarafından hazırlanan bu bilgi grafiğine bakın).
- Orta derecede: Hastalık ilerledikçe hastalarda hafıza kaybı ve kafa karışıklığı, iletişim ve okuma güçlüğü, giyinme gibi rutin işlerde zorluk, aile ve arkadaşları tanımada sorunlar, paranoya, halüsinasyonlar ve gezinme artar.
- Şiddetli: Ağır Alzheimer hastalarında iletişim kuramama, kilo kaybı, yutma güçlüğü ve bağırsak ya da mesane kontrolü kaybı görülür. Bu aşamada hastalar çoğu zaman yataktadır ve bakımları için tamamen başkalarına bağımlıdırlar.
Alzheimer hastalarının yaşadıkları zorluklar çok büyüktür, çünkü hastalık günlük yaşamlarını her yönüyle etkilemektedir. Aşağıda hastalar veya hastaların arkadaşları ve aileleri tarafından yazılan birkaç hikayeyi okuyabilirsiniz.
Eski bir diş hekimi ve Harvard'da yardımcı doçent olan Sandy, unutkanlığının daha da kötüye gittiğini fark etmesiyle ilgili olarak CNN muhabirlerine şunları söyledi: "'Bir buçuk saat boyunca bir diş vakası dosyasına bakıyorum' diye hatırlıyor. 'Okuyorum, beynimin içinde. Sonra dosyayı kapatıyorum ve vaka hakkında kelimenin tam anlamıyla hiçbir şey hatırlamıyorum'." Kısa bir süre sonra kendisine Alzheimer hastalığı teşhisi kondu.
Eşine Alzheimer hastalığı teşhisi konan Fred Walker, Alzheimer's Research UK'e eşi hakkında konuştu: "'Telefon kullanmak onun yeteneklerinin ötesine geçti. Tüm düğmelere hakim olamıyordu. Ocak anlamak için çok karmaşıktı ve her zaman gazı açık bırakma tehlikesi vardı. Bir fincan çay yapmayı çok zor buluyordu ve ne kadar çay, süt ve su gerektiği konusunda kafası karışıyordu."
Alzheimer hastalığı, ileri evrelere ulaştığında ve bunamaya doğru ilerlediğinde, Alzheimer Derneği için Laury tarafından tanımlanmıştır:
"[...] yeni bir yolculuğa çıktık. Bu yolculuk 24 saat bakım, günlük ilaç vizitleri ve annemin kendi zihninin sisinde tamamen kaybolmasını içeriyordu. [...] O ana kadar bu acımasız, sinsi hastalığa yakalanmış bir sevdiğini izlemenin ne kadar büyük bir dehşet gösterisi olduğunu anlayamamıştı. [...] Halüsinasyon görmeye başladı."
everyone.org un kurucusu Sjaak Vink bu tanımların her birini doğruluyor ve tanıyor. Annesine 2015 yılında Alzheimer teşhisi konmuş.
Bu, hastalar ve sevdikleri için zor bir yoldur ve hastalık sadece onların kişisel yaşamlarını ve sevdiklerinin yaşamlarını etkilemekle sınırlı değildir.
Bakıcılar, bütçeler ve politika yapıcılar üzerindeki baskı
Alzheimer hastaları, durumları kötüleştikçe evde bakım, gece bakımı, temizlik hizmetleri veya hemşirelik bakımı gibi giderek daha zorlu bir bakıma ihtiyaç duyarlar; sonunda hastaların destekli yaşam tesislerinde veya bakım evlerinde yaşamaları gerekebilir. Hastalık, hastaya, (genellikle kendilerini hastaya bakmaya adayan) aile üyelerine, kişisel ve devlet bütçelerine ağır bir yük getirir.
Aile bakıcıları, Alzheimer hastası sevdiklerine bakarken zor bir görevle karşı karşıya kalmaktadır. Yapılan bir anket, Birleşik Krallık'taki aile bakıcılarının %95 'inin bu durumun fiziksel veya ruhsal sağlıklarını etkilediğini, %69'unun sürekli yorgun, %64'ünün endişeli ve %49'unun depresif hissettiğini ortaya koymuştur.
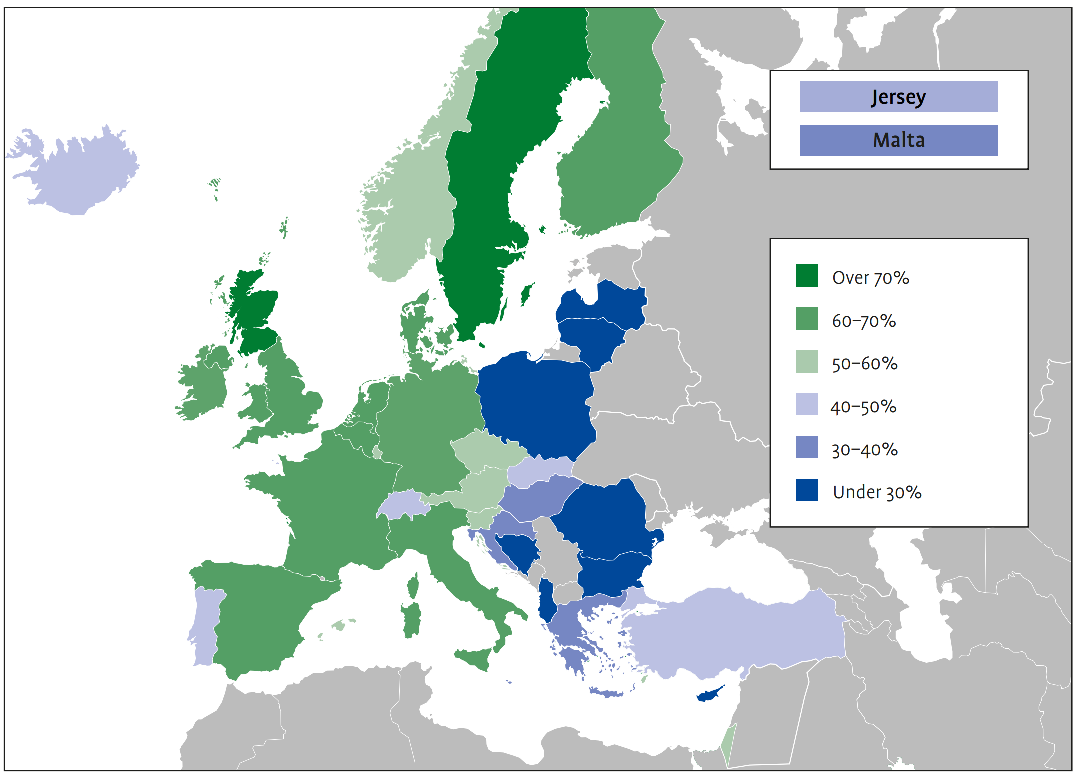
Avrupa'da Alzheimer hastalığı ve diğer demans türleri yaklaşık 10 milyon kişiyi etkilemektedir ve bu sayının 2030 yılına kadar 14 milyona çıkması beklenmektedir. Avrupa'da demansın ekonomik maliyetinin 2030 yılına kadar 250 milyar Euro'nun üzerine çıkacağı ve bunun %50'sinden fazlasının gayri resmi bakım maliyetlerinden kaynaklanacağı tahmin edilmektedir. Bakım ve tedaviye erişim eşitsizdir ve özellikle Doğu Avrupa'da Alzheimer hastaları ve bakıcıları için mevcut destek sistemleri ve sosyal programlar eksiktir.
Amerika Birleşik Devletleri'nde Alzheimer hastalığı yakın zamanda ilk 10 ölüm nedeni listesine girmiştir ve ilk 10'da bilinen bir tedavisi olmayan tek hastalıktır. ABD'de 6 milyon kişiyi etkilemektedir ve bu sayının 2050 yılına kadar 12 milyona çıkacağı tahmin edilmektedir. 2021 yılı sonu itibariyle Alzheimer ve diğer demanslarla yaşayan insanlara bakmanın toplam ulusal maliyeti 355 milyar dolara ulaşabilir ve 2050 yılına kadar 1,1 trilyon dolara ulaşacağı tahmin edilmektedir.
Astronomik gibi görünen bu fon, hastalara yeterli destek ve mümkün olduğunca onurlu bir yaşam sunmak için gereklidir.
Alzheimer hastaları, özellikle ilerleyen aşamalarda, günün her saati bakım gerektirdiğinden, birçok ülkede veya toplumda olduğu gibi, bakımları yetersiz olduğunda özellikle etkilenmektedir. Sadece Birleşik Krallık'ta her yıl on binlerce demans hastası, yetersiz bakımdan kaynaklanan enfeksiyonlar, düşmeler ve dehidrasyon nedeniyle acil servise başvurmaktadır. Bu da ulusal sağlık bütçelerini daha da zorlamaktadır.
COVID-19 salgını sırasında, Alzheimer hastaları ciddi şekilde etkilenmiş ve yaş, diğer uzun vadeli sağlık koşulları ve Alzheimer'ın kendi zorlukları (örneğin, hastaların COVID-19 enfeksiyonlarını önleyen yönergeleri takip etmekte zorlanmasına neden olan hafıza sorunları ve kafa karışıklığı) nedeniyle yüksek bir ölüm oranına maruz kalmıştır.
Bakım evlerindeki Alzheimer hastaları, bunun zarar verici sonuçlarını başka şekillerde de hissetmiştir. Yetersiz bakım ve onları COVID-19'dan korumak için sevdiklerinden ayrılmaya zorlanmaları nedeniyle, ortaya çıkan yalnızlık ve izolasyon zihinsel ve fiziksel sağlıklarını daha da kötüleştirmiştir.
Sağlık ve ekonomik krizlerin ciddi boyutlara ulaşmasını engellemek için de hastalığa yönelik etkili tedavilere ihtiyaç duyulmaktadır.
Alzheimer hastalığı araştırmalarında öne çıkan noktalar
1910 yılında Almanya'da bir doktor olan Emil Kraepelin, derin hafıza kaybı ve kötüleşen psikolojik değişiklikleri olan bir hastada presenil demansın patolojik özelliklerini keşfeden doktor Alois Alzheimer'dan sonra bu duruma "Alzheimer hastalığı" adını verdi. Alzheimer hastalığının tedavisine yönelik araştırmalar ancak 1980'lerin sonunda Amerika Birleşik Devletleri'nde başlamış, ancak doktorlar hala Alzheimer'ın yaşlanmanın kaçınılmaz bir sonucu olduğuna inandıkları için eleştirilerle karşılaşmışlardır.
Amerika Birleşik Devletleri'nde 1978 yılında Ulusal Yaşlanma Enstitüsü (NIA) ve Alzheimer Derneği, Pfizer ile ortaklık kurarak Alzheimer hastalığının semptomlarını tedavi edecek bir ilaç için ilk klinik çalışmayı başlattı. İlaç 1993 yılında onaylanmıştır: Cognex (tacrine), yayınlanan sonuçlara göre, bazı hastalarda bilişsel yetenekleri geliştirdi, ancak hastalığın kötüleşmesini durdurmadı.
Sonraki on yıl içinde, hepsi Alzheimer hastalığının bilişsel semptomlarını tedavi etmek için altı ilaç daha onaylandı:
- Aricept (donepezil): hafıza ve düşünme ile ilgili semptomların tedavisi için
- Razadyne (galantamin): hafıza ve düşünme ile ilgili semptomların tedavisi için
- Exelon (rivastigmin): hafıza ve düşünme ile ilgili semptomların tedavisi için
- Namenda (memantin): hafızayı, dikkati, mantığı ve dili geliştirmek için
- Namzaric (memantin + donepezil): yukarıdakilerin bir kombinasyonu
- Belsomra (Suvorexant): Alzheimer hastalarında uykusuzluk tedavisi için
Alzheimer hastalığının tedavisi için onaylanan son ilaç 2003 yılında onaylanmıştır. On yıllar boyunca Alzheimer hastalığı yaşlanmanın doğal bir sonucu olarak kabul edildi. Gerçek bir hastalık olup olmadığı tartışıldığından, bir tedavi bulmak için çok az kaynak ayrılmıştır. Ancak son 20 yılda araştırmacılar hastalığı incelemek ve bir tedavi geliştirmek için geniş kaynaklar ayırdılar.
Alzheimer'a yönelik tedavilerin eksikliği ilaç şirketlerinin ihmalinden kaynaklanmamaktadır - sektör genel olarak araştırmalara milyarlarca dolar yatırım yapmıştır. Sadece Eli Lilly şirketi başarılı bir ilaç geliştirmek için otuz yıl boyunca 4,2 milyar dolar harcadı ve Amerika Birleşik Devletleri Ulusal Sağlık Enstitüleri (NIH) tedavileri araştırmak ve geliştirmek için yılda 500 milyon dolardan fazla para harcadı.
Amerika Birleşik Devletleri Kongresi, 2013 yılından bu yana NIH'in Alzheimer araştırmaları ve ilgili demanslar için ayırdığı yıllık bütçeyi üç katına çıkararak 2019 yılında 3,1 milyar dolara ulaştırmıştır.
Ulusal ve özel fonlar, 2019 yılına kadar çeşitli teorileri test etmek için 2173 klinik araştırmanın yapılmasını sağlamıştır. Test edilen en önemli teoriler:
- Çalışmaların %19'u bir nörotransmitter hipotezine odaklanmıştır
- Çalışmaların %17,0'ı mitokondriyal kaskad hipotezini ve diğer ilgili hipotezleri test etmiştir
- 12,7'si tau yayılımı hipotezini test etmiştir
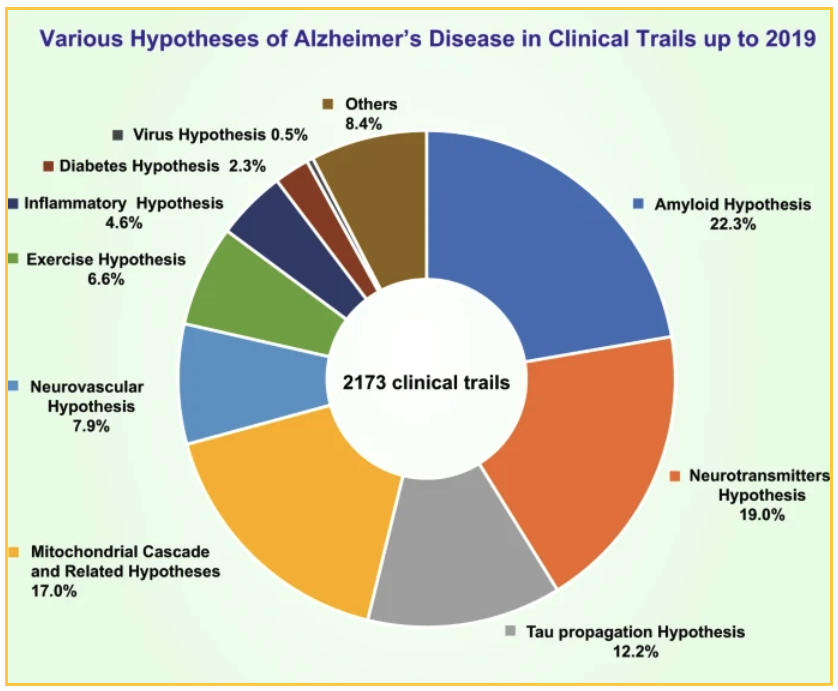
Amiloidi hedef alan çalışmaların %22,3'ü plağı azaltmanın farklı yollarına odaklanmaktadır:
- Beta-amiloid için bağışıklık sistemi tarafından üretilen antikorlar: Vücuda enjekte edildiğinde bağışıklık sistemini tetikleyerek beta-amiloidi yok edecek antikorlar üreten ve beyindeki beta-amiloid seviyelerini azaltan "aktif aşılar".
- Beta-amiloid için laboratuvarda üretilen antikorlar: Vücutta antikor üretimini tetiklemeye çalışmaktan daha etkili ve daha güvenli olduğu düşünülen "pasif aşılar".
- Beta-amiloid üretiminin azaltılması: Bazı deneysel tedaviler, beta-amiloid üretimini önleyebilen veya azaltabilen belirli proteinlerin davranışını değiştirir.
- Beta-amiloid agregasyonunu önleme: Bilim insanları, beta-amiloid ile beyin hücreleri arasında beyin hücresinin ölümüne yol açan ilk etkileşimleri önleyen ilaçları araştırıyor.
- Beta-amiloid giderimini arttırmak: Beta-amiloid'e saldırmak için bağışıklık sistemini harekete geçirmek veya anti-amiloid etkileri olan doğal ajanlar uygulamak gibi teknikler.
- Anti-amiloid etkileri olan doğal ajanlar: İnsan kan bağışçılarından elde edilen intravenöz immünoglobulin (IVIg), beta-amiloid seviyelerini azaltabilen doğal antikorlar içerir.
Aduhelm aducanumab-avwa) nedir?
Aduhelm (aducanumab), Alzheimer hastalığının tedavisi için endike bir anti-amiloid antikordur. Alzheimer hastalığı olan hastalarda beyin hücreleri arasında anormal miktarlarda oluşan ve etkilenen beyin hücrelerinin ölümüne yol açan beta-amiloid plaklarını ortadan kaldırmak için tasarlanmıştır. Beta-amiloid 1984 yılında tanımlanmış ve kısa sürede beyin hücresi hasarının ana tetikleyicisi olarak kabul edilmiştir. 1986 yılında ise yumakların temel bileşeni ve beyin hücresi bozulmasının ikinci tetikleyicisi olan tau proteini tanımlanmıştır.
Aduhelm , merkezi Massachusetts, Amerika Birleşik Devletleri'nde bulunan çok uluslu bir biyoteknoloji şirketi olan Biogen, Inc. tarafından geliştirilmiştir. Aduhelm aylık enjeksiyon olarak uygulanmaktadır.
Aduhelm 'in uzun bir geçmişi vardır.
İsviçreli biyoteknoloji şirketi Neurimmune Therapeutics AG, Zürih Üniversitesi ile işbirliği içinde, sağlıklı yaşlılarda ve yavaş ilerleyen demans hastalarında koruyucu anti-amiloid antikorları tanımladı ve Aduhelm'in aktif bileşeni olan aducanumab'ın keşfedilmesini sağladı. Hafif Alzheimer hastalığı olan hastalarda, bir yıllık aylık intravenöz aducanumab infüzyonları amiloid plağını azaltmakta ve bu da bilişsel gerilemenin yavaşlamasına neden olmaktadır.
Neurimmune, Alzheimer hastalığının tedavisi için aducanumab'ı 2007 yılında Biogen'e lisanslamıştır ve geliştirme konusunda Biogen ile işbirliği içinde çalışmaktadır.
Aduhelm nasıl çalışır?
Alzheimer hastalığı, beta-amiloid ve tau adlı iki proteinin beyinde olağandışı bir şekilde birikmesi sonucu ortaya çıkmaktadır. Beta-amiloid, normalde beyinde bulunan ve Alzheimer hastalığında beyin hücreleri arasında amiloid plaklar halinde kümelenen bir proteindir - amiloid teorisi, bu plakların beyin hücrelerine zarar verdiğini ve sonunda öldürdüğünü belirtir. Amiloid plakları hastalığın erken dönemlerinde gelişirken, tau yumakları hastalığın ilerleyen dönemlerinde ortaya çıkma eğilimindedir. Alzheimer hastalığına bir tedavi bulmak için yapılan araştırmaların çoğu amiloid plaklarını ortadan kaldırmaya odaklanmıştır.
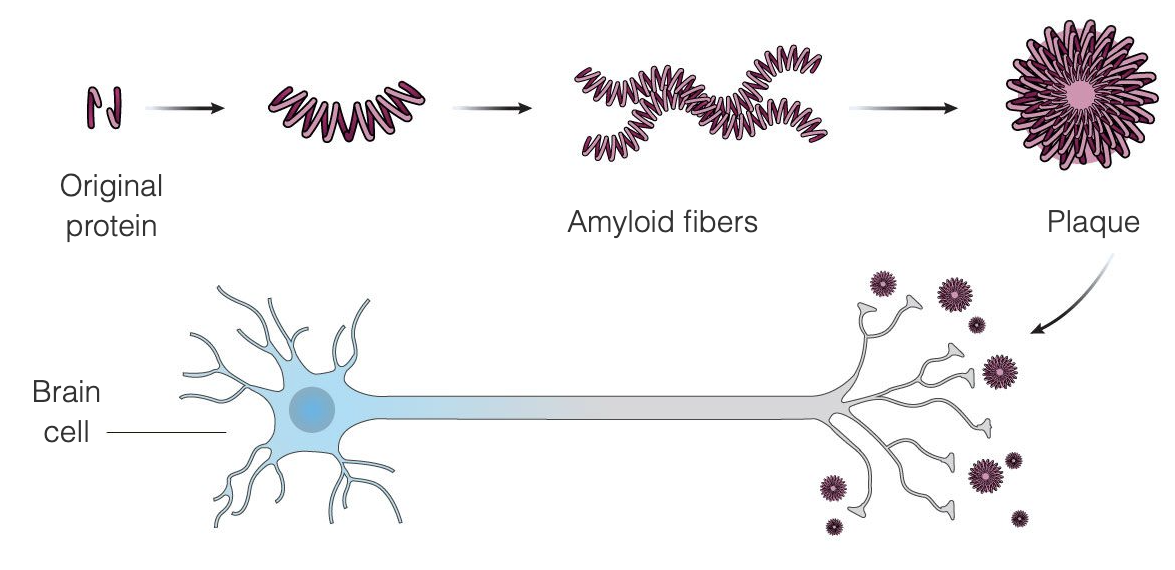
Aduhelm , amiloid plaklarına bağlanarak Alzheimer'ı hastalığın çok erken aşamalarında tedavi etmek için tasarlanmıştır, böylece bağışıklık sistemini yabancı bir istilacı olarak görerek plakları yok etmesi için tetikler. Amaç, plaklar ortadan kaldırıldığında beyin hücrelerinin ölmeyi bırakması ve bilişsel işlevlerin kötüleşmesinin durmasıdır. Aduhelm bu mekanizmayı hastalığın ilerlemesini yavaşlatmak amacıyla kullanmakta ve özellikle Alzheimer hastalığının erken evrelerindeki hastalara hitap etmektedir. Aduhelm , halihazırda meydana gelmiş olan hasarı tersine çevirmez.
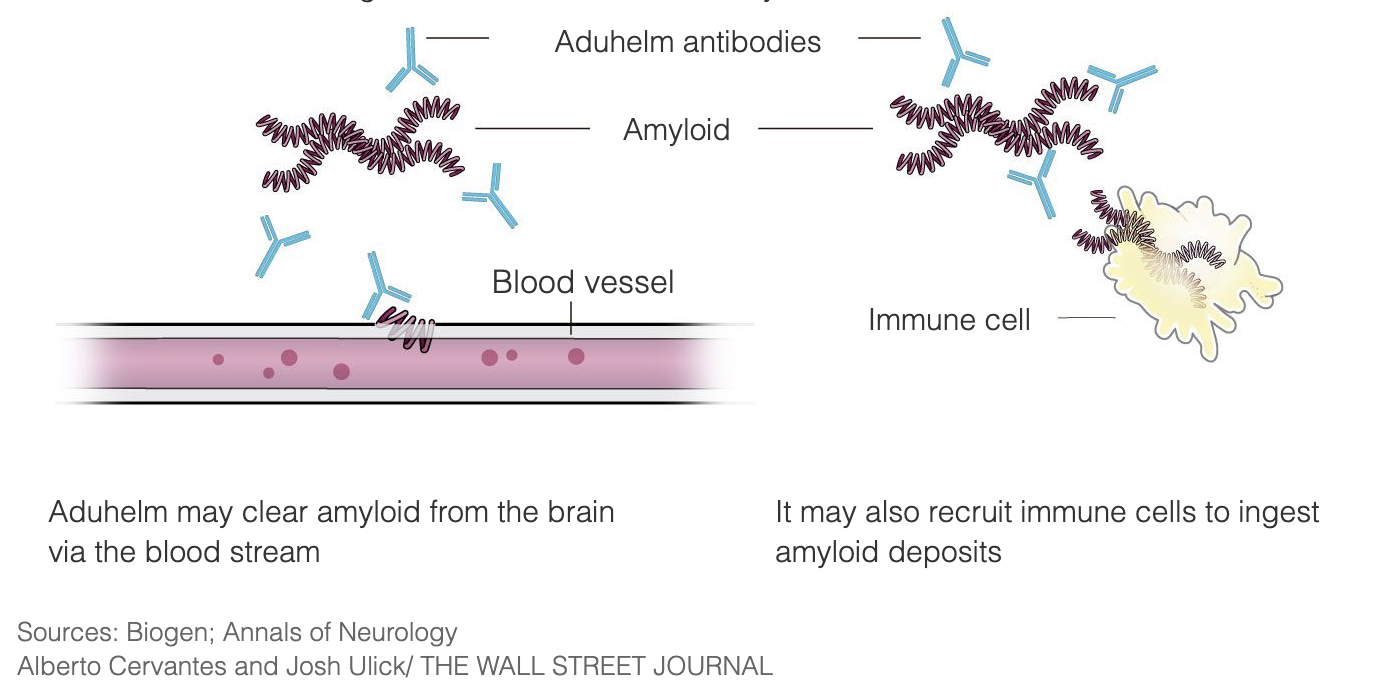
Amiloid plaklar, otuz yıldır Alzheimer hastalığı araştırmalarının ve ilaç geliştirmenin hedefi olmuştur ve Aduhelm , yıllar boyunca araştırılan bu tür tedavilerden biridir.
"Kutsal Amiloid Kilisesi"
Bilim insanları Alzeimer hastalığına neyin sebep olduğu konusunda henüz hemfikir değiller, ancak bazı teorileri var. Bunlardan biri "amiloid hipotezi" olarak adlandırılıyor ve Aduhelm bu teorinin doğru olduğu varsayımı üzerine geliştirildi.
Amiloid hipotezi, beyin hücreleri arasında oluşan amiloid plaklarının hücrelerin ölümüne neden olduğunu ve bunun da bilişsel gerilemeye yol açtığını belirtmektedir. Bu, hiçbir zaman evrensel olarak kabul görmemiş uzun soluklu bir teoridir ve amiloid plaklarını hedef alan klinik çalışmaların şimdiye kadarki başarısızlığı, teoriyi eleştirenleri cesaretlendirmiştir. Bazıları, alternatif teorileri değerlendirmeyi reddetmeye varan isteksizlikleri nedeniyle teorinin destekçileri grubunu "Kutsal Amiloid Kilisesi" olarak adlandırıyor.
Beta-amiloidin beyindeki normal işlevi bile araştırmacılar tarafından tartışılmaktadır, çünkü insan vücudunda doğal olarak nasıl bir rol oynadığı veya kesinlikle Alzeimer hastalığının bir belirteci olup olmadığı konusunda hemfikir değillerdir.
Amiloid hipotezine yönelik yaygın bir karşı argüman, normal bilişsel becerilere sahip birçok yaşlı insanın beyninde plaklar bulunmasıdır. İlginç bir şekilde, 90 yaşın üzerinde olağanüstü anılara sahip bazı kişilerin ölüm sonrası muayenelerinde beyinlerinde farklı derecelerde amiloid plakları tespit edilmiştir - bazılarında Alzheimer'ın en şiddetli vakalarına benzeyecek kadar yüksek yoğunluk vardı ve ayrıca Alzheimer ile ölen insanlardan çok daha fazla nöron vardı.
Bazı araştırmacılar beta-amiloidin aslında koruyucu bir rolü olabileceğine inanmaktadır.
San Antonio'daki Texas Üniversitesi'nde nörobiyolog olan George Perry, "beta-amiloid ve tau birikiminin aslında hücrede yaşa bağlı metabolik baskılara karşı koruyucu bir yanıt olduğunu" ve özellikle beyindeki oksidatif stresi azaltmada yardımcı olduğunu öne sürüyor (oksidatif stres yaşla birlikte artar ve bu da hücrelere zarar verir).
Çeşitli çalışmalar Alzheimer hastalığının diğer potansiyel nedenlerini araştırmıştır. Bu çalışmalardan biri, New York Mount Sinai'deki Icahn Tıp Fakültesi'ndeki araştırmacılar tarafından yürütülmüş ve HHV (herpesvirüs ailesinin bir parçası) adı verilen bir virüsün iki türünün Alzheimer hastalığı olan kişilerin beyinlerinde daha büyük miktarlarda bulunduğunu keşfetmiştir. Bu iki virüsün hastalığa neden olduğu kesin olmasa da (daha büyük olasılıkla neden virüs artı APOE adı verilen belirli bir gen varyantının kombinasyonudur), veriler enfeksiyonun Alzheimer'a yakalanma riskini artırdığını ve antiviral ilaçlarla tedavi edilen kişilerin Alzheimer'a yakalanma olasılığının on kat daha az olduğunu göstermektedir.
Bununla birlikte, amiloid teorisini destekleyen genetik bulgular, amiloid ile ilgili gen problemlerini erken başlangıçlı Alzheimer hastalığının (30 ila 65 yaş arası kişilerde) gelişimine bağlamaktadır. Down sendromu bir risk faktörü olarak kabul edilmektedir, çünkü araştırmacılar Down sendromlu kişilerin erken başlangıçlı Alzheimer hastalığı ile bağlantılı bir amiloid proteinini kodlayan geni içeren bir kromozomun fazladan bir kopyasına sahip olduğunu bulmuşlardır.
Diğer genetik anormallikler, daha kolay plak oluşturan daha uzun beta-amiloid varyantlarının üretimine yol açabilir veya beta-amiloid üretimini artırabilir ve biraz nadir görülen erken başlangıçlı Alzheimer hastalığı vakalarına neden olabilir. Bir ailede birden fazla aile üyesi bu gen mutasyonlarını taşıyabilir ve bir bireyin erken başlangıçlı Alzheimer geliştirme riskini artırabilir.
Amiloid teorisini destekleyenler, amiloid plaklarını hedef alan ilaçları içeren önceki denemelerin basitçe kusurlu olduğunu öne sürmektedir. Örneğin, beta-amiloid proteinlerinin üretimini engelleyen semagacestat ile ilgili bir çalışmada, katılımcıların bilişsel durumları kötüleşmiş; araştırmacılar ayrıca katılımcılar arasında cilt kanserinin arttığını gözlemlemişlerdir. Bunun nedeni, semagacestat'ın sadece beta-amiloid değil, bazıları insan vücudunda önemli işlevlere sahip olan diğer proteinlerin üretimini de engellemesi olabilir.
Amiloidleri hedef alan bu denemelerin başarısızlığı için en çok desteklenen açıklama, ilaçların doğru ilaçlar olduğu, ancak Alzheimer hastalığının ilerlemesinde yanlış noktada uygulandığıdır - semptomların ortaya çıkmasından onlarca yıl önce başlayan bir süreç olan amiloid plakları oluşturma sürecinde çok geç uygulanmaktadırlar.
Kentucky Üniversitesi'nde sinirbilimci olan Michael Murphy, " 50'li yaşlarındaki insanlara verdiğimiz takdirde Alzheimer hastalığını tedavi edebilecek bir ilaca muhtemelen zaten sahip olduğumuzu" belirtiyor.
Alzheimer'ın nedenleri hakkında önemli tartışmalar var ve uzmanlar henüz aynı fikirde değil - ancak hastalar ve araştırmacılar, Aduhelm'in Faz 3 klinik deneylerinden birinde aducanumab'ın sonuçlarıyla yeni bir rüzgar yakaladı.
Klinik deneylerde Aduhelm
Klinik araştırmalar dört aşamada gerçekleşir:
- Faz 0: İlaç, zararlı olmadığından ve denemenin devam edebileceğinden emin olmak için 15'ten az katılımcı üzerinde çok küçük miktarlarda test edilir.
- 1. Aşama: İlaç, ciddi bir yan etkisi olmadığından emin olmak için altta yatan sağlık sorunları olmayan 20 ila 80 katılımcı üzerinde test edilir. FDA'ya göre, ilaçların yaklaşık %70 'i Faz 2'ye geçmektedir.
- Faz 2: İlaç, etkinliği ve yan etkileri hakkında bilgi toplamak için birkaç ay veya yıl boyunca ilacın amaçlandığı rahatsızlığa sahip yüzlerce katılımcı üzerinde test edilir. İlaçların yaklaşık %33'ü 3. Aşamaya geçer.
- 3. Aşama: İlaç, ilacın amaçlandığı rahatsızlığa sahip 3000'e kadar katılımcı üzerinde test edilir ve birkaç yıl sürebilir. İlacın güvenli ve etkili olduğu kanıtlanmalıdır. İlaçların %25-30'u 4. Aşamaya geçer.
- 4. Aşama: Bu aşama uzun yıllar boyunca binlerce katılımcıyı içerir ve FDA ilacı onayladıktan sonra gerçekleşir. Amacı, uzun vadeli güvenliği ve etkinliği hakkında daha fazla bilgi toplamaktır.
Aduhelm 1. Aşamada
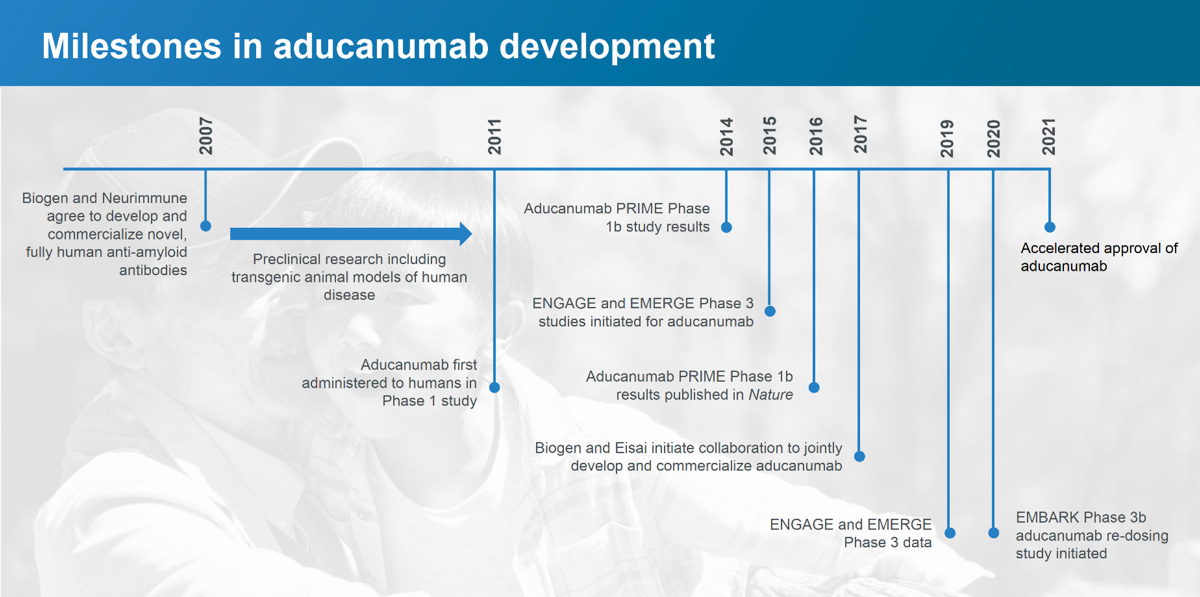
Biogen, 2011 yılında aducanumab'ı sağlıklı gönüllülerde ve ABD ve Japonya'daki Alzheimer hastalarında farklı dozlarda aducanumab ve plasebo ile test eden üç Faz 1 çalışmasından başlayarak aducanumab'ı araştıran çeşitli klinik çalışmalar yürütmüştür. Bazı hastalar 3 yıldan uzun bir süre boyunca kayıt altına alınmıştır.
2016 yılında Biogen, araştırmacıların hafif Alzheimer hastalığı olan deneme katılımcılarına bir yıl boyunca aylık intravenöz aducanumab infüzyonları uyguladıkları Faz 1 klinik çalışmalarının sonuçlarını yayınladı. Aducanumab ile tedavi edilen katılımcıların beynindeki beta-amiloid seviyeleri azalmış ve resmi Klinik Demans Derecelendirmesi ile ölçülen bilişsel gerileme yavaşlamıştır. Biogen'in araştırmacıları aducanumab infüzyonu alan katılımcılar arasında ARIA (amiloidle ilişkili görüntüleme anormallikleri, örneğin beyin ödemi veya beyinde kanama) gibi yan etkilerde de azalma kaydetti. Biogen bu sonuçları Faz 2'ye geçmek için yeterince cesaret verici buldu.
Aduhelm 2. Aşamada
Biogen, 2018'in sonlarında Faz 2 denemelerine başlamış ve erken evre ve semptomatik Alzheimer hastalığı olan katılımcılarda amiloid plakların azalmasını ve bilişsel gerilemenin yavaşlamasını kontrol etmenin yanı sıra aducanumab dozunun devam etmesinin güvenliğini değerlendirmiştir.
Aducanumab, 12. ayda daha yavaş bilişsel gerileme gösterme konusundaki birincil hedefinde başarısız oldu, ancak denemeden elde edilen 18 aylık veriler bir yeniden analizde gözden geçirildikten sonra, aducanumab'ın en yüksek dozu olan beş dozdan birinde olumlu etkiler gözlendi. En yüksek dozun beyindeki amiloid plaklarını azalttığı ve biliş üzerinde olumlu tepkiler gösterdiği gösterilmiştir.
Faz 1'de olduğu gibi, tüm katılımcıların yaklaşık %10'unda ARIA (amiloid ile ilişkili görüntüleme anormallikleri) ve en yüksek adukanumab dozlarını alan katılımcılarda %15'ten daha az yan etki gözlenmiştir.
Cleveland Clinic Lou Ruvo Beyin Sağlığı Merkezi kurucu direktörü Jeff Cummings, Biospace için yaptığı açıklamada, "BAN2401 çalışmasının 18 aylık sonuçları etkileyici ve amiloid hipotezi için önemli bir destek sağlıyor.
Aduhelm 3. Aşamada
Faz 2 çalışmasının sonuçlarının ardından Biogen, Kuzey Amerika, Avustralya, Avrupa ve Asya'da nispeten hafif Alzheimer hastalığı olan 3300'den biraz daha az katılımcının kaydedildiği Engage ve Emerge adlı iki Faz 3 çalışması yürütmüştür. Aducanumab, kan dolaşımına enjeksiyon yoluyla düşük ve yüksek dozlarda ayda bir kez uygulandı ve plasebo alan katılımcıların sonuçları ile karşılaştırıldı.
Mart 2019'da Biogen, bağımsız bir veri izleme komitesi tarafından yürütülen ve adukanumabın amaçlandığı gibi çalışmadığı sonucuna varan bir yararsızlık analizini gerekçe göstererek iki Faz 3 çalışmasını durdurmuştur.
Karar 3300 çalışma katılımcısını etkiledi. Çalışmaya katılma protokolleri sık ve uzun ziyaretleri içeriyordu ve kan alımı, MRI'lar, PET taramaları ve bazen spinal muslukları içeriyordu. İki çalışmanın durdurulmasından yedi ay sonra Biogen, ek verilerin yeniden analizinin, ilacın yüksek dozlarda bilişsel gerilemeyi azalttığını gösterdiğini duyurdu.
Biogen bir basın açıklamasında, ek verilerin Faz 3 Engage çalışmasında yüksek doz aducanumab alan ve bilişsel ve işlevsel bozukluklarda (hafıza, oryantasyon, dil) önemli ölçüde azalma ve günlük yaşamdaki aktivitelerde (ev işleri, alışveriş, bağımsız olarak ev dışına seyahat etme) faydalar yaşayan bir hasta alt kümesinden elde edilen sonuçlardan oluştuğunu yazdı. Bu sonuçlara dayanarak Biogen, Ekim 2019'da aducanumab için ruhsatlandırma onayı başvurusunda bulundu ve Haziran 2021'in başlarında onay aldı.
Faz 3 klinik çalışmaları, tedavinin biliş ve işlev açısından faydaları konusunda tam olarak kesin olmasa da FDA, çalışmaların Aduhelm ticari adıyla üretilen aducanumab'ın amiloid plakları azaltabildiğini gösterdiği sonucuna varmış ve bu da FDA'nın hızlandırılmış onay kararının temelini oluşturmuştur.
Deneme katılımcısı ve muhabir Phil Gutis, Being Patient haber platformu için şunları yazdı: "Boylamsal bir çalışma olan PET taraması sayesinde beynimde artık amiloid bulunmadığını öğrendim. Penn Memory Center'daki Aging Brain Cohort çalışmasının bir parçası olarak yaklaşık iki yıl önce çekilen bu tarama, aducanumab'ın bana gerçekten yardımcı olduğuna dair artan sezgilerimi doğruladı. Sürekli bir zihinsel sisten çıkıyormuş gibi hissetmeye başladım... Olumsuz tarafı ise, kaybettiğim anılarım geri gelmedi."
Aduhelm'in yan etkileri ve kontrendikasyonları
Biogen'in İlaç Kılavuzu'na göre, Aduhelm'i düşünmeden önce, hastalar sağlık hizmeti sağlayıcılarını, aşağıdakiler de dahil olmak üzere tüm tıbbi durumları hakkında bilgilendirmelidir:
- hamileyseniz veya hamile kalmayı planlıyorsanız
- emziriyorsanız veya emzirmeyi planlıyorsanız
Hastalar, reçeteli ve reçetesiz ilaçlar, vitaminler ve bitkisel takviyeler de dahil olmak üzere aldıkları tüm ilaçları sağlık hizmeti sağlayıcılarına bildirmelidir.
Biogen İlaç Rehberi'ne göre, Aduhelm 'in bilinen ana yan etkisi ARIA (amiloid ile ilişkili görüntüleme anormallikleri), beyin ödemi ve beyinde kanamadır. Diğer yan etkiler şunlardır:
- yüz, dudak, ağız veya dilde şişme ve kurdeşen gibi ciddi alerjik reaksiyonlar
- baş ağrıları
- İSHAL
- konfüzyon/deliryum/değişmiş zihinsel durum/disoryantasyon
- düşüyor
ARIA, genellikle herhangi bir belirtiye neden olmayan, ancak ciddi olabilen yaygın bir yan etkidir. En yaygın olarak beyinde geçici bir şişlik olarak görülür ve genellikle zamanla kendiliğinden düzelir. Aynı zamanda, amiloidin beyinden uzaklaştırılması kan damarlarından amiloidi de uzaklaştırır, bu da beynin içinde veya yüzeyinde küçük kanama noktaları oluşturabilir.
Klinik çalışmalarda adukanumab alan katılımcıların %41 'inde ARIA gözlenirken, plasebo alan katılımcıların %10'unda ARIA gözlenmemiştir.
Beyin bölgelerinde şişme olan çoğu kişide belirti görülmese de, insanların yaklaşık %30'unda aşağıdaki gibi hafif belirtiler görülebilir:
- Karışıklık
- baş ağrıları
- baş dönmesi
- görüş değişiklikleri
- Mide bulantısı
Emekli nörolog ve Aduhelm klinik çalışmalarının uzun süreli katılımcısı Daniel Gibbs, son derece nadir görülen bir ARIA yan etkisiyle ilgili deneyimini paylaştı:
"Öncelikle şunu söylemeliyim ki bu büyük ölçüde doğru olan bir dogmadır, [ARIA'lar] genellikle iyi huyludur. Çoğu insan kendisinde olduğunu bilmez. [ARIA'lar] sadece MR taramalarında küçük şişlik alanları ya da kanamadan kaynaklanan küçük demir birikimi alanlarının olduğu yerlerde yakalanır. Eğer insanlarda semptomlar varsa, bunlar genellikle hafiftir. Baş ağrısı en yaygın olanıdır, bazen de kafa karışıklığı.
Ancak neredeyse her zaman, semptomatik ARIA'da bile, ilacı bırakırsanız, birkaç ay içinde kaybolurlar. İlaç güvenli bir şekilde yeniden başlatılabilir. En azından ilacın üreticisi Biogen tarafından tartışılan çok az sayıda feci ARIA veya ciddi ARIA vakası olmuştur ve benimki de bu kategorideydi. [...]
Baş ağrılarımda bir artış olmaya başladı. Baş ağrılarım nadiren olmaz, bu yüzden gerçekten bir şey düşünmedim, ancak biraz daha sık ve belki biraz daha şiddetli hale geldiler, ancak yine de reçetesiz satılan [ilaçlarla] rahatladılar. [...]
Sonra 2017 Noel'inden bir ya da iki gece önce hayatımın en kötü baş ağrısını yaşadım, nörologlar olarak subaraknoid kanama ile ilişkilendireceğimiz türden, beyinde büyük kanama. Kan basıncımı ölçtüm ve çok yüksekti ve yüksek kalmaya devam etti, bu yüzden felç geçirdiğimi düşündüm.
Eşim beni acil servise götürdü ve yerel hastanemize vardığımda gerçekten tutarlı bir öykü veremiyordum. [...]
Ama birkaç gün içinde biraz daha iyiydim. Baş ağrım geçti ama hala okumakta zorlanıyordum. Sonraki ay biraz daha kötüleşti. O zamanki MR taramalarım, beynimin her yerinde hem şişlik hem de kanama ile bunun ARIA olduğunu gösterdi. Arttığı için tedavi edilmesi gerektiği düşünüldü. Beş doz yüksek doz steroid aldım ve bu baş ağrısı ve kafa karışıklığını hemen giderdi. Ancak beynimdeki şişliğin tamamen geçmesi yaklaşık altı ay sürdü."
Bu nadir ancak ciddi potansiyel yan etkiler ışığında, hastaların sağlık hizmeti sağlayıcılarının ARIA'yı kontrol etmek için Aduhelm ile tedavi öncesinde ve sırasında manyetik rezonans görüntüleme (MRI) taramaları yapması gerekecektir.
Aduhelm 'in (aducanumab) onaylanması
7 Haziran 2021'de FDA, Alzheimer hastalığının tedavisi için Aduhelm 'e (aducanumab) hızlandırılmış onay verdi.
Hızlandırılmış onay, klinik çalışmalarda olumlu bir terapötik etki gösteren ilaçlara, tüm kesin kanıtlar sunulmadan önce verilebilen bir onay türüdür. Bu, yalnızca karşılanmamış bir tıbbi ihtiyacı karşılayan ciddi durumlara yönelik ilaçlar için geçerli olabilir; Alzheimer hastalığının tedavisi için onaylanan son ilaç 18 yıldan daha uzun bir süre önce onaylanmıştır.
Hızlandırılmış onay şartlı olarak verilmiştir. FDA, üretici Biogen'den ilacın klinik faydasını doğrulamak için yeni bir klinik araştırma yapmasını talep etmektedir. Araştırma fayda göstermezse, FDA ilacın onayını geri çekebilir. Biogen'in aducanumab'ın Alzheimer hastaları için faydalarını doğrulamak üzere başka bir klinik araştırmayı tamamlamak için 2029 yılına kadar süresi var; uzmanlar, iki yılda tamamlanabilecek üçüncü bir klinik araştırmanın, hastalar pahalı bir tedaviye girip en iyisini umarken ilacın işe yarayıp yaramadığını öğrenmek için sekiz yıl beklemekten daha iyi bir seçenek olacağını savunuyor.
Mali boyutları olan tıbbi bir tartışma
FDA'nın aducanumab'ı onaylama kararı, Aduhelm 'in Alzheimer hastalığı için etkili bir tedavi olduğuna dair yeterli kanıt olmadığını söyleyen uzmanları şaşırttı. Bağımsız bir panel de dahil olmak üzere bu uzmanların birçoğu FDA'ya mevcut kanıtların aducanumab'ın bilişsel gerilemeyi yavaşlatabileceğine dair önemli şüpheler uyandırdığını bildirmiş ve iki Faz 3 çalışmasından yalnızca birinden elde edilen olumlu sonuçların FDA onayı için yeterli bir dayanak olup olmadığını tartışmıştır.
Onaydan kısa bir süre sonra üç bilim adamı, ikna edici kanıtların eksikliğini gerekçe göstererek FDA'ya tedavi konusunda tavsiyelerde bulunan bağımsız komiteden protesto amacıyla istifa etti. Bu bilim insanları ayrıca FDA'nın adukanumabın erken evre Alzheimer hastaları üzerinde denenmesine ve amiloid plağının azaltılmasının bilişsel semptomları yavaşlatacağı teorisinin kabul edilmesine rağmen (bilim camiasının bu teorinin geçerliliği konusundaki görüş ayrılığına rağmen) Alzheimer hastası olan herkes için onaylama kararını eleştirdi.
FDA'nın aducanumab'ı bu koşullar altında onaylama kararının çeşitli sonuçları olabilir.
- Eli Lilly'nin donanemab'ı gibi amiloid plaklarını hedef alan diğer ilaçlar, daha önce tahmin edilenden daha hızlı onay alabilir ve ilaç şirketlerinin Alzheimer ilaçlarına yatırım yapma veya mevcut denemelere katılımlarını sürdürme konusundaki ilgisini artırabilir.
- FDA'nın kararı, diğer biyoteknoloji şirketlerini nadir görülen durumlar için ilaç geliştirmeye teşvik edebilecek bir düzenleme esnekliği algısı yarattı; bu dürtü, özellikle Alzheimer tedavilerinin onaylanması arasındaki 18 yılda, uzun bir dizi klinik deney başarısızlığının ardından söndü.
- İlaç yıllık 56.000 $ ile oldukça maliyetlidir, bu da sigortacıların ödemesi beklendiğinden özel sağlık sigortası oranlarının artabileceği ve Medicare'in (ABD ulusal sağlık sigortası) bir parçası olarak vergi mükellefleri üzerindeki yükü artıracağı anlamına gelmektedir. Bazıları bunun Medicare için sadece temel maliyetleri nedeniyle değil, aynı zamanda Aduhelm ile tedavi, hastaların amiloidi tespit etmek için spinal musluklarla daha erken teşhis edilmesini ve MRI'larla (diğerlerinin yanı sıra) sürekli izlenmesini gerektirdiği için "yıkıcı" olabileceğini söylüyor, bu da maliyetleri önemli ölçüde artırıyor ve tıbbi sistemler üzerinde baskı oluşturuyor.
Onay, hisseleri %50'den fazla yükselen Biogen için de bir talih kuşu olarak görülürken, Japon ortağı Eisai Co'nun hisseleri %56 yükseldi. Analistler, sadece ABD'de Alzheimer hastalığı teşhisi konmuş 6 milyon kişi olduğu düşünüldüğünde, Aduhelm 'in potansiyel olarak 10 milyar dolarlık satış yapabileceğini tahmin ediyor. Rekabet, multipl skleroz (MS) için Tecfidera ve spinal musküler atrofi (SMA) için Spinraza ilaçlarının satışlarına zarar verdiği için ilaç Biogen'in büyümesi için önemli.
Spinraza , Biogen'in portföyünde yer alan ve tedavinin ilk yılı için 750.000 $ ve sonraki her yıl için 375. 000 $ 'lık liste fiyatıyla yüksek fiyat etiketine sahip bir başka ilaçtır.
FDA'nın Aduhelm'i onaylama kararını herkes eleştirmiyor
Alzheimer ilerleyici bir hastalık olduğundan, hastaların tedaviye geç değil erken ihtiyacı vardır. FDA'nın kararıyla ilgili haberler, tedavinin kendileri ya da sevdikleri için işe yarayacağı ya da diğer şirketleri başka Alzheimer tedavileri geliştirmek için harekete geçireceği konusunda birçok kişiye yeni bir umut verdi.
Hasta savunucusu gruplar, zayıflatıcı hastalık için sadece birkaç ay boyunca semptomları ele alan sadece altı başka tedavi mevcut olduğu için onay için şiddetle bastırmışlardı. Kasım 2020'de FDA'nın danışma komitesi Aduhelm'in onaylanmasına karşı oy kullanmış, bu da Alzheimer Derneği'nde önce öfkeye sonra da harekete geçmeye yol açmış, dernek daha sonra ilacın potansiyelini desteklediklerini ifade etmek ve umut ve ilerleme ihtiyacını vurgulamak için kampanya başlatmıştır.
Ocak 2021'de FDA ve hasta grupları, hastaların, hasta bakıcıların, klinisyenlerin ve savunucuların tedaviyi desteklediği bir dinleme oturumunda bir araya geldi ve diğer şeylerin yanı sıra hastaların bir tedavi için daha fazla beklemeyi göze alamayacağını savundu.
FDA Yeni İlaçlar Ofisi Direktörü Peter Stein bir basın toplantısı sırasında hasta görüşlerinin bir rol oynadığını doğruladı. FDA'nın "hastalardan, hepimizin bildiği gibi çok yıkıcı sonuçları olabilen bu hastalığın ilerlemesini önlemede anlamlı fayda sağlayabilecek bir ilaca erişebilmek için bazı belirsizlikleri kabul etmeye istekli olduklarını çok net bir şekilde duyduğunu" söyledi.
FDA'nın İlaç Değerlendirme ve Araştırma Merkezi'nin müdür vekili Patrizia Cavazzoni, aynı basın toplantısında "verilerin hastaların ve bakıcıların bu ilacı kullanma seçeneğine sahip olmalarını desteklediğini" söyledi.
Alzheimer Derneği'nin baş bilim sorumlusu Maria Carrillo, "Bu FDA ilaç onayı Alzheimer tedavisi ve araştırmalarında yeni bir dönemi başlatıyor" dedi. "Tarih bize yeni bir kategorideki ilk ilacın onaylanmasının alanı canlandırdığını, yeni tedavilere yapılan yatırımları artırdığını ve daha fazla yeniliği teşvik ettiğini göstermiştir."
Aduhelm Avrupa'da ne zaman onaylanacak?
Alzheimer hastalığı, yüzyılın en büyük tıbbi, ekonomik ve sosyal krizlerinden biri olarak hızla yükseliyor ve özellikle Avrupa'da tanıyı doğrulayabilecek uzmanların eksikliği göz önüne alındığında, erken teşhis edilmesi zor bir hastalık. Sadece Avrupa'da 2018 yılı itibariyle 9,7 milyon kişi Alzheimer hastalığı ve diğer demans türlerinden muzdariptir; 2030 yılına kadar hasta sayısının 14 milyona çıkacağı tahmin edilmektedir ve bu da etkili tedavilere ciddi bir ihtiyaç yaratmaktadır.
Aduhelm henüz Amerika Birleşik Devletleri dışında onaylanmamıştır. Biogen, Ekim 2020'de Avrupa Birliği'nde ve 2020 yılı sonunda Japonya, Kanada, Avustralya ve Brezilya'da ruhsatlandırma incelemesi için başvuruda bulunmuştur.
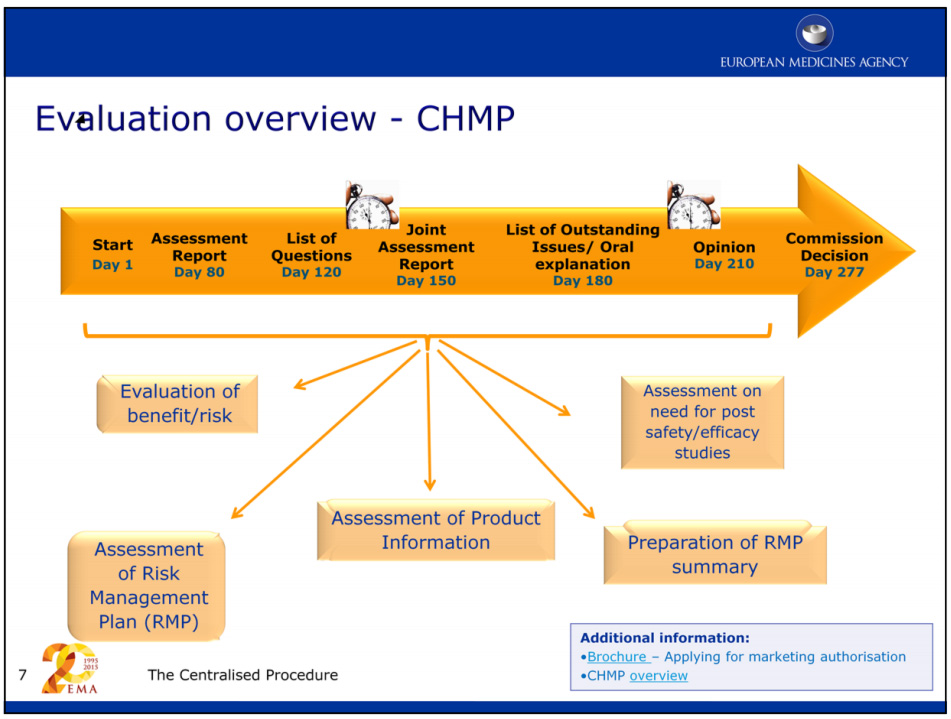
Avrupa İlaç Ajansı'na (EMA) göre, yeni bir ilacın ruhsat başvurusunun değerlendirilmesi genellikle yaklaşık bir yıl sürmektedir; ilaç geliştiricisine Hızlandırılmış Değerlendirme verilmişse bu süre daha da kısalmaktadır.
Bu yılın Mart ayında Biogen'in İsviçre'deki 2 milyar dolarlık üretim tesisi, İsviçre Terapötik Ürünler Ajansı'ndan (Swissmedic) İyi Üretim Uygulamaları (GMP) lisansı aldı. Biogen, 2021'in sonlarında İsviçre'deki tesiste Aduhelm üretmek için FDA onayı almayı planlıyor ve ilacı yılda 1 milyondan fazla hastaya tedarik etmeyi bekliyor.
Aduhelm 'e Amerika Birleşik Devletleri dışından erişim
Aduhelm şu anda FDA onaylıdır ve Amerika Birleşik Devletleri'nde ikamet edenler için mevcuttur - ve ilaçların şu anda onaylanmadıkları ülkelerde ithal edilmesine izin veren düzenlemeler vardır.
Hayatı tehdit eden veya zayıflatıcı hastalıkları olan hastalar, tedavi eden doktorlarının yardımıyla ilaçlara erişme, satın alma ve ithal etme hakkına sahiptir.
Hastalar ve doktorları bunu, bir ilaca normalde ancak hastanın yaşadığı ülkede piyasa izni/onayı (hangi ifadeyi kullanırsak kullanalım) alındıktan sonra erişilebileceğine dair genel kuralın yasal bir istisnası olan merhametli kullanım veya isimli hasta ithalat düzenlemeleri temelinde yapabilirler. Bu istisna, hastaların kendi ülkelerinde henüz onaylanmamış ilaçlara yasal, etik ve güvenli bir şekilde erişmelerine ve almalarına olanak tanır.
"Adlandırılmış hasta esası" hakkında daha fazla bilgiyi buradan (EMA) edinebilirsiniz.
everyone.org , hastaların ve onları tedavi eden hekimlerin mümkün olan en iyi tedavi için dünya çapında mevcut olan her türlü ilaca erişebilmelerini taahhüt eder. Amerika Birleşik Devletleri dışındaysanız, ülkenizdeki düzenlemeler dahilinde %100 uyumlu bir şekilde faaliyet gösteriyoruz. Daha fazla ayrıntı okumak, ilaca erişmek veya destek ekibimizle iletişime geçmek istiyorsanız, bunu buradan yapabilirsiniz.
Aduhelm 'in fiyatı ne kadar?
Biogen, ortalama bir hasta için idame dozunda (10 mg/kg) Aduhelm maliyetinin yılda 56.000 $ olacağını açıkladı. Buna hastaların tedavi öncesinde ve tedavi sırasında yaptırmak zorunda oldukları testler dahil değildir.
Biogen, ilacın yıllık yüksek fiyatı konusunda eleştiriler almıştır.
İlaç fiyatlarını analiz eden kar amacı gütmeyen Klinik ve Ekonomik İnceleme Enstitüsü (ICER), adil bir yıllık fiyatın her yıl hasta başına 2.500 ila 8.300 dolar arasında değişeceğini belirtti. ICER yaptığı açıklamada, FDA'nın onayının hastaları korumada başarısız olduğunu ve Biogen'in "hastaların tedaviden gerçek faydalar elde ettiğini doğrulayacak kanıtları beklerken bile" yılda 50 milyar dolardan fazla para toplayabileceğini söyledi.
Biogen CEO'su Michel Vounatsos, ilacın fiyatının hastalara ve Alzheimer'ın daha az yükünü çeken bir topluma getireceği değerle gerekçelendirildiğini ve fiyatın "yirmi yıldır yenilik yapılmamasının" bir yansıması olduğunu ileri sürerek eleştirilere yanıt verdi. "Tedaviye yatırım yapmanın zamanı geldi" diye ekledi.
everyone.org olarak, Biogen tarafından belirlenen fiyatı etkileyemeyiz. Hastaların Aduhelm 'e aşağıdaki fiyatlardan erişmelerine yardımcı olabiliyoruz:
- 170 mg/1,7 mL'lik (100 mg/mL) bir flakon için 1.958,58 €
- Bir flakon 300 mg/3 mL (100 mg/mL) için 3.046,68 €
Daha fazla bilgi için buradan talepte bulunun.
Alzheimer hastalığı için yaklaşan tedaviler
Mayıs 2021'de yayınlanan bir çalışma, şu anda Alzheimer hastalığı için klinik çalışmalarda 126 tedaviolduğunu göstermektedir. Bunların %82,5'i hastalık modifikasyonunu hedeflerken, %10,3'ü bilişi geliştirmekte ve %7,1'i nöropsikiyatrik semptomları hafifletmeye odaklanmaktadır.
- Faz 3 çalışmaları: 28 tedavi (aducanumab dahil)
- Faz 2 denemeleri: 74 tedavi
- Faz 1 denemeleri: 24 tedavi
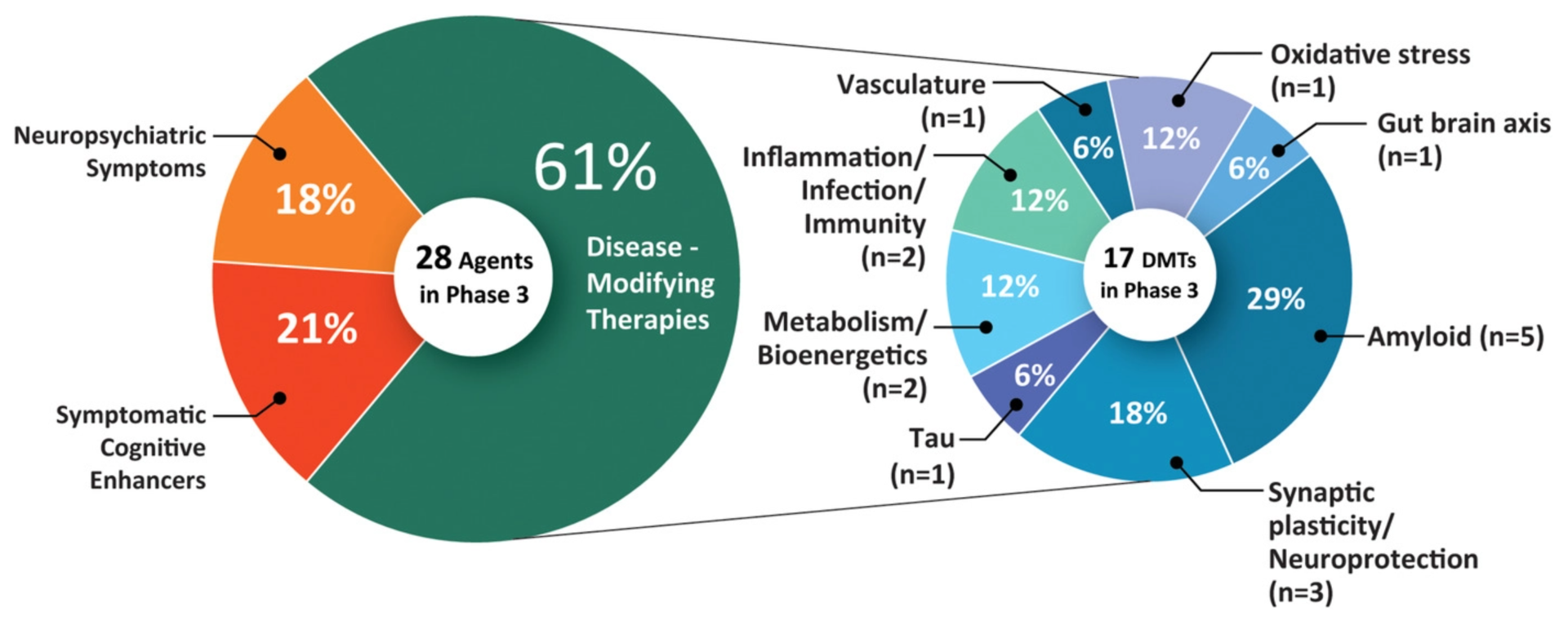
Faz 3 denemelerindeki tedavilerin büyük olasılıkla önümüzdeki yıl onaylanması bekleniyor.
Lecanemab
Yayınlanan raporlara göre, aducanumab ile benzer bir şekilde çalışan (beta-amiloid plakları ortadan kaldırmak için bağışıklık sistemini tetikleyen) monoklonal antikor lecanemab umut vaat ediyor ve Faz 3 klinik denemelerine geçti.
Gantenerumab
Gantenerumab beta-amiloid'e, özellikle de kanda dolaşan tekil beta-amiloid'e kıyasla beta-amiloid plaklarına bağlanır. Bir hücrenin belirli bir molekülü kendi içine alıp sindirdiği bir süreç olan fagositozu uyararak amiloid plaklarını çözdüğü ve beta-amiloidi uzaklaştırdığı düşünülmektedir. Gantenerumab'ın önceki klinik çalışmaları, doğrudan gen mutasyonlarından kaynaklanmayan daha yaygın Alzheimer formuna sahip kişilerde beta-amiloid plakları azalttığını göstermiştir. İki büyük küresel Faz III çalışmasında incelenmeye devam etmektedir.
Solanezumab
Solanezumab, beta-amiloidi kan ve beyin omurilik sıvısından "temizlemeyi" ve böylece plak oluşumunu önlemeyi amaçlayan bir antikordur. Yararlar, denemelerin üç buçuk yıllık süresinin tamamında yer alan katılımcılarda bildirilmiştir ve daha sonra katılan katılımcılarda daha az bildirilmiştir, bu nedenle etkileri hakkında öğrenilecek daha çok şey vardır.
Donanemab
Donanemab, Alzheimer tedavisi için gelecek vaat eden bir başka ilaç gibi görünüyor. Eli Lilly and Company tarafından test edilmekte olan bu ilaç, daha küçük çaplı çalışmasının sonuçlarını teyit etmek amacıyla 1500 katılımcıyı büyük bir çalışmaya kaydetmeyi planlamaktadır; 76 hafta süren ve 257 hastayı kapsayan bu önceki çalışma, raporlara göre donanemabın Alzheimer hastalığının ilerlemesini önemli ölçüde yavaşlattığını göstermiştir.
Diğerleri
Saracatinib, beta-amiloid plaklarının oluşumuna yardımcı olan Fyn kinaz adlı bir proteinin inhibitörü olarak görev yapan deneysel bir bileşiktir. Fareler üzerinde yapılan bir çalışma, saracatinib'in Fyn kinazı inhibe ederek farelerde hafıza kaybını tersine çevirmede etkili olduğunu göstermiştir. Fyn kinaz inhibisyonu hastalığın ilerlemesini önleyebilir veya geciktirebilir.
Kaliforniya'daki Salk Biyolojik Çalışmalar Enstitüsü'ndeki araştırmacılar fisetin adlı bir kimyasal üzerinde çalışıyorlar ve beyin hücrelerinin kaybını yavaşlatmada etkili olduğunu tespit ettikleri CMS121 adlı bir fisetin versiyonu geliştirdiler. Bir ilacın onaya hazır hale gelmesi için daha fazla araştırma yapılması gerekiyor.
Aduhelm'in son onayı ile ilgili olarak, ABD'nin Chicago kentindeki hasta-savunuculuk grubu Alzheimer's Association'ın Baş Bilim Sorumlusu Maria Carrillo, Nature için yaptığı açıklamada şunları söyledi: "Umutluyuz ve bu hem bu ilaç hem de Alzheimer için daha iyi tedaviler içinbir başlangıç."
"Gerçekte olduğumuz tek şey düşüncelerimiz ve beynimizdir." - Sandy, eski diş hekimi ve yardımcı doçent ve Alzheimer hastası.
everyone.org olarak, bilimin insan ırkını ileriye taşıdığına ve hayatları iyileştirdiğine ve hatta kurtardığına inanıyoruz. Alzheimer hastalığı pek çok kişinin yaşam kalitesini tehlikeye atıyor. Kendilerini (çözümün bir parçasını) bulmaya adamış bilim insanlarını sebat etmeye teşvik ediyoruz ve umut verici sonuçlar gösteren geliştirilmekte olan tedavilerin önümüzdeki 3 yıl içinde onaylanmasını ve dünyanın dört bir yanındaki Alzheimer hastaları için erişilebilir hale gelmesini dört gözle bekliyoruz.




