Leqembi ve Aduhelm arasındaki fark nedir? Basit bir genel bakış.
Son güncelleme: 19 Kasım 2024
Ülkenizde onaylanmamış olsalar bile yeni ilaçlara yasal olarak erişebilirsiniz.
Nasıl olduğunu öğreninFDA, 2021'den bu yana iki yeni Alzheimer ilacına hızlandırılmış onay verdi. Bu ilaçlar anti-amiloid tedavileri olan Leqembi (lecanemab) ve Aduhelm (aducanumab). Her iki onay da Alzheimer tedavisinde büyük atılımların olmadığı neredeyse 20 yılın ardından geldi. Bu nedenle her iki ilaç da medyada geniş ilgi gördü.
Ancak tepkiler karışık olmuştur. Alzheimer Derneği'nin Baş Bilim Sorumlusu Maria Carrillo, yeni ilaçların onaylanmasını "bu tedaviye uygun kişiler için bir dönüm noktası" olarak nitelendirdi [2]. Aynı zamanda, onay süreçleri, özellikle Aduhelm'da olduğu gibi, tartışmalarla çevrili olmuştur [1, 4].
Bir hasta olarak, muhtemelen Leqembi (lecanemab) ve Aduhelm (aducanumab) arasındaki farkın ne olduğunu merak ediyorsunuzdur. Bu makalede, iki ilacı çalışma şekilleri, etkinlikleri, maliyetleri ve bulunabilirlikleri açısından karşılaştıracağız.
Leqembi vs Aduhelm: Ne için kullanılırlar?
Her iki ilaç da erken Alzheimer hastalığına yönelik tedavilerdir. Bunlar anti-amiloid tedavilerdir ve beyindeki amiloid plaklarını hedef alırlar.
Reçeteleme bilgilerine göre, Leqembi ve Aduhelm hafif bilişsel bozukluğu olan ve beta-amiloid seviyelerinin yükseldiği teyit edilen hastalar için tasarlanmıştır [5].
Leqembi vs Aduhelm: Nasıl çalışırlar?
Benzerlikler
Leqembi (lecanemab) ve Aduhelm (aducanumab) monoklonal antikorlardır. Alzheimer hastalarının beyinlerinde biriken beta-amiloid plakları hedef almak üzere tasarlanmışlardır. Bu plakların, bu hastalıkta görülen bilişsel gerileme ve klinik düşüşe katkıda bulunduğuna inanılmaktadır.
Her iki ilaç da hastalığın ilerlemesini yavaşlatmak amacıyla amiloid plaklarına bağlanır ve nötralize eder. Leqembi ve Aduhelm 'u galantamin, rivastigmin ve donepezil gibi önceki Alzheimer tedavilerinden temelde farklı kılan da budur. Bu önceki tedaviler hastalığın semptomlarını hafifletmeye odaklanmaktadır. Leqembi ve Aduhelm ise hastalığın temel nedenini hedef alarak hastalığın seyrini değiştirmeyi amaçlamaktadır.
Farklılıklar
Leqembi ve Aduhelm beta-amiloid proteininin farklı kısımlarına bağlanır. Aduhelm daha büyük, sertleşmiş amiloid plaklarına daha güçlü bağlanır. Leqembi'nin amiloid proteininin daha küçük, çözünür (ve daha toksik) formunu daha iyi hedeflediği bildirilmektedir [6].
Leqembi ve Aduhelm ne kadar verimlidir?
Leqembi (lecanemab) ve Aduhelm(aducanumab)'ın etkinliği klinik çalışmalarda incelenmiştir.
-
Leqembi klinik araştırma sonuçları
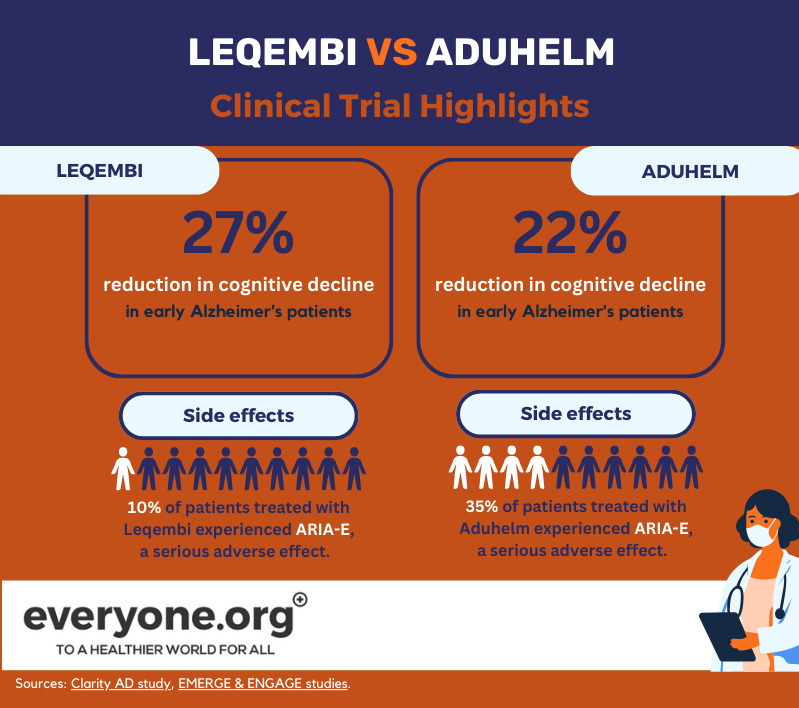
Leqembi'nin hızlandırılmış FDA onayı, Faz 3 Clarity AD çalışmasından elde edilen olumlu üst düzey sonuçlara dayanmaktadır. Bu sonuçlara göre, Lecanemab erken Alzheimer hastalarında plaseboya kıyasla bilişsel gerilemeyi %27'ye kadar yavaşlatmıştır. Bu sonuçlar tedaviye başladıktan 18 ay sonra ölçülmüştür [8].
Çalışma sonuçlarına ilişkin ek bir analiz Nisan 2023'te yayımlanmıştır. Bu analiz, hastaların 9 ila 59 aylık bir süre boyunca Leqembi almayı bıraktıktan sonra bile bilişsel gerilemedeki gecikmeden faydalanmaya devam ettiklerini göstermiştir. Bu "boşluk dönemi" sırasında, orijinal klinik çalışmada Leqembi alan hastalarda Alzheimer hastalığının plasebo alanlara kıyasla sürekli olarak daha yavaş bir oranda ilerlediği görülmüştür [7].
ARIA-E'nin ciddi advers etkisi Leqembi ile tedavi edilen hastaların %10'unda meydana gelmiştir. Çalışmadaki hastaların %6'sında bir başka ciddi yan etki olan ARIA-H görülmüştür [13].
-
Aduhelm kli̇ni̇k araştirma sonuçlari
FDA hızlandırılmış onayını Aduhelm adresine iki Faz 3 klinik çalışma temelinde vermiştir. Bunlardan biri (EMERGE) hastaların klinik gerilemesinde %22'ye varan bir azalma göstermiştir [12]. Diğeri (ENGAGE) ise göstermedi. Ancak her iki çalışmada da Aduhelm beyindeki amiloid plaklarında azalma olduğunu göstermiştir [9]. FDA bu endikasyonun "klinik fayda sağlama olasılığının makul derecede yüksek" olduğuna karar vermiştir [10].
FDA'nın talebi doğrultusunda Haziran 2022'de bir Faz 4 doğrulama çalışması (ENVISION) başlatılmıştır. Sonuçların 2026 yılında alınması beklenmektedir [9].
Aduhelm'un reçete bilgilerine göre, klinik çalışmalarda ilacı alan hastaların %35'i ARIA-E yaşamıştır. Deneme hastalarının %34'ü ARIA-H yaşamıştır [15].
Mevcut verilerin gösterdiği gibi, bu noktada Leqembi ve Aduhelm arasındaki temel fark güvenlik profillerinde görünmektedir ve Leqembi daha düşük bir advers etki insidansı göstermektedir.
Aynı zamanda, mevcut klinik çalışma verilerine dayanarak, Leqembi'nin bilişsel gerileme üzerinde daha tutarlı bir etki sağladığı görülmektedir. Hem Leqembi hem de Aduhelm üzerinde devam eden denemelerin sonuçları, her iki ilacın performansı hakkında daha fazla netlik sağlayacaktır.
NOT Burada paylaşılan sonuçlar bilgilendirme amaçlıdır ve bir tedavi seçiminin temeli olarak kullanılmamalıdır. Doktorunuz sizin durumunuza en uygun tedaviyi belirlemek için en iyi konumdadır.

Leqembi vs Aduhelm: Güvenlik ve yan etkiler
Reçeteleme bilgilerine göre, Leqembi (lecanemab) ve Aduhelm'un en yaygın yan etkileri şunlardır:
Leqembi yan etkileri
- Ateş, grip benzeri semptomlar, bulantı, işitme hızında değişiklikler ve nefes darlığı dahil olmak üzere infüzyonla ilişkili reaksiyonlar;
- Baş ağrısı;
- Amiloidle İlişkili Görüntüleme Anormallikleri (ARIA) [13]. ARIA beyinde geçici şişme veya kanamayı içerebilir. ARIA'nın belirtileri baş ağrısı, kafa karışıklığı, nöbetler, yürüme güçlüğü ve baş dönmesidir. Homozigot apolipoprotein E geni taşıyıcılarında ARIA riski daha yüksek olabilir [14].
Aduhelm yan etkiler
Aduhelm 'un en yaygın yan etkileri ARIA, baş ağrısı ve düşmedir. Aduhelm için belirtilen ancak Leqembi için belirtilmeyen bir advers reaksiyon aşırı duyarlılıktır. Aşırı duyarlılık reaksiyonları anjiyoödem (derinin daha derin katmanlarının şişmesi) ve ürtikeri (deri döküntüsü) içerebilir [15].
Leqembi vs Aduhelm: Fiyat karşılaştırması
Henüz yaygın olarak bulunmayan ilaçlar söz konusu olduğunda, herhangi bir fiyatı yalnızca bir gösterge olarak almalısınız. Nihai maliyetler bulunduğunuz yere, tedarikçilere veya sigorta kapsamına bağlı olarak değişme eğilimindedir.
Bir fikir vermesi açısından, tek dozluk bir Leqembi flakonunun maliyeti yaklaşık 1.043 Avro'dur. İlacın iki haftada bir uygulanması önerildiğinde, bu 1 kişi için yıllık maliyeti yaklaşık 27.118 Avro'ya çıkarmaktadır [16].
Tek dozluk flakon başına Aduhelm 'un gösterge fiyatı 1.335 Avro'dur. Bu, 1 kişi için yıllık maliyet açısından 34.710 Avro'ya denk gelmektedir [17].
Leqembi ve Aduhelm nerede onaylanmıştır?
Leqembi (lecanemab) şu anda sadece ABD ve Birleşik Krallık'ta onaylanmıştır ve EMA onayının 2024'ün sonuna kadar alınması beklenmektedir[3]. Leqembi ayrıca Çin ve Japonya'da da ruhsat başvurusunda bulunmuştur [18, 19, 20].
Aduhelm (adukanumab) Haziran 2021'de ABD'de FDA tarafından hızlandırılmış onay almıştır. Avrupa İlaç Ajansı (EMA) Aralık 2021'de Aduhelm'un pazarlama başvurusunu reddetti. Başvuru daha sonra Biogen tarafından Nisan 2022'de geri çekilmiştir [21]. Japonya Sağlık Bakanlığı da Aduhelm'un ülkedeki onayı hakkında olumsuz bir sinyal gönderdi [22].
Leqembi veya Aduhelm ülkenizde (henüz) onaylanmadı mı veya mevcut değil mi? Siz ve doktorunuz bu tedavilerin size fayda sağlayabileceğini düşünüyorsanız, tıbbi erişim uzmanlarından oluşan ekibimizle iletişime geçin. İlacı sizin için tedarik etmek üzere size kişiselleştirilmiş bir fiyat teklifi verebiliriz.
Referanslar:
- Anti-amiloid monoklonal antikor Lecanemab: 16 uyarı notu. Zenodo, 3 Ocak 2023.
- Hamilton, Jon. FDA Alzheimer ilacı Leqembi'ye hızlandırılmış onay verdi : Shots - Sağlık Haberleri. NPR, 6 Ocak 2023.
- FDA Danışma Kurulu, LEQEMBI® (lecanemab-irmb)'nin Alzheimer Hastalığının Tedavisinde Klinik Yararını Oybirliğiyle Onayladı. Biogen | Yatırımcı İlişkileri, 9 Haziran 2023.
- Helmore, Edward. FDA, Alzheimer ilacının onaylanması nedeniyle ateş altında Aduhelm. The Guardian, 29 Aralık 2022.
- REÇETELEME BILGILERININ ÖNEMLI NOKTALARI. Leqembi, Erişim tarihi: 3 Ağustos 2023.
- Taylor, Emma. Yeni Alzheimer tedavisi lecanemab manşetlere çıktı: sırada ne var? Alzheimer's Research UK, 13 Aralık 2022.
- Eisai: Alzheimer hastaları Leqembi'nin faydalarını durdurulduğunda bile görüyor. CNBC, 6 Nisan 2023.
- Leqembi | ALZFORUM. Alzforum, 30 Mayıs 2023, Erişim tarihi: 3 Ağustos 2023.
- Aduhelm | ALZFORUM. Alzforum, 6 Şubat 2023, Erişim tarihi: 3 Ağustos 2023.
- Cavazzoni, Patrizia. FDA'nın Alzheimer Hastalığı için Yeni Tedaviyi Onaylama Kararı. FDA, 7 Haziran 2021.
- Eisai, lecanemab'ın Clarity AD Faz III çalışmasının tam sonuçlarını sunuyor. Alzheimer Avrupa, 30 Kasım 2022.
- EMERGE ve ENGAGE Topline Sonuçları: Erken Alzheimer Hastalığı Olan Hastalarda Aducanumab'ı Değerlendirmeye Yönelik İki Faz 3 Çalışması. Biogen | Yatırımcı İlişkileri, Erişim Tarihi: 3 Ağustos 2023.
- Referans Kimliği: 5105416. Accessdata.fda.gov, Erişim tarihi: 3 Ağustos 2023.
- İLAÇ REHBERİ LEQEMBI® (leh-kem'-bee) (lecanemab-irmb) enjeksiyonu, intravenöz kullanım için. Leqembi, Erişim tarihi: 3 Ağustos 2023.
- REÇETELEME BILGILERININ ÖNEMLI NOKTALARI. Accessdata.fda.gov, Erişim tarihi: 3 Ağustos 2023.
- Leqembi (lecanemab-irmb) Online Satın Alın - Fiyat & Maliyetler. Everyone.org, Erişim tarihi: 3 Ağustos 2023.
- Aduhelm ( aducanumab-avwa)Online Satın Alın - Fiyat ve Maliyetler. Everyone.org, Erişim tarihi 3 Ağustos 2023.
- EISAI, AVRUPA'DA ERKEN ALZHEIMER HASTALIĞI TEDAVİSİ OLARAK LECANEMAB İÇİN PAZARLAMA YETKİSİ BAŞVURUSUNU SUNMUŞTUR | Biogen. Biogen | Yatırımcı İlişkileri, 10 Ocak 2023.
- Eisai, Çin'de Lecanemab için BLA Veri Sunumunu Başlattı | Biogen. Biogen | Yatırımcı İlişkileri, 22 Aralık 2022.
- Carvalho, Teresa ve Ray Burow. Erken Alzheimer için Lecanemab Japonya'da İncelemeye Alınıyor. Alzheimer's News Today, 14 Mart 2022.
- Avrupa Birliği'nde Aducanumab için Ruhsatlandırma Başvurusuna İlişkin Güncelleme | Biogen. Biogen | Yatırımcı İlişkileri, 22 Nisan 2022.
- Swift, Rocky ve diğerleri. Eisai-Biogen Alzheimer ilacının değerlendirilmesi zor-Japonya bakanlığı. Reuters, 22 Aralık 2021.